
先看结论(给忙的人30秒读完)

- 很多CAR-T/罕见病研究最终卡住的,不是方案设计,而是随访断链与数据不可追溯。
- 要降低脱落率、减少清洗返工、提高证据输出效率,关键是把研究管理做成患者全生命周期的数据闭环:采集有标准、过程有留痕、质控可追踪、输出可复盘。
- 落地优先抓三件事:ePRO+自动提醒(不断链)、字段模板+校验规则(少返工)、关键动作证据链(可审计)。
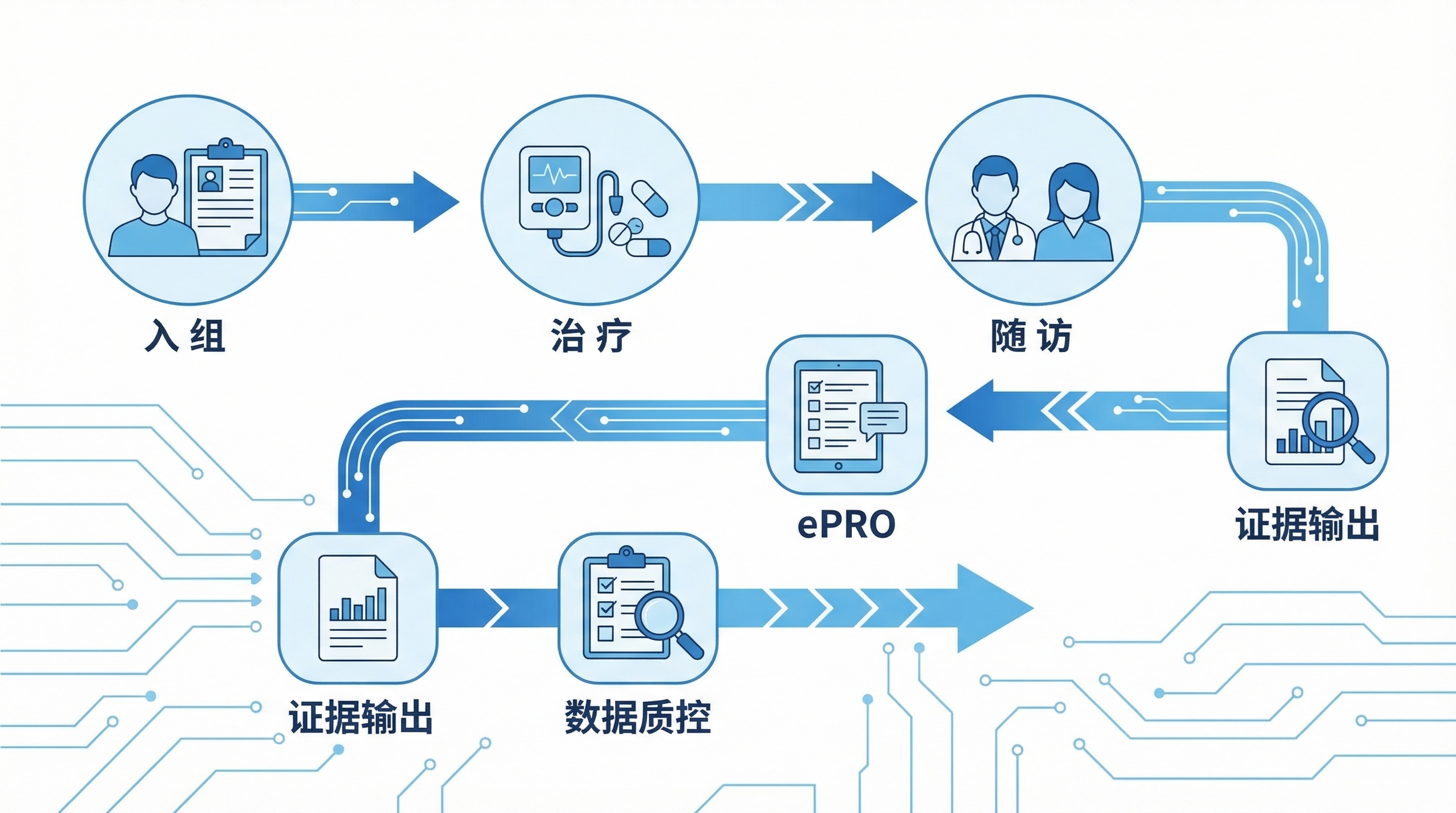
为什么很多研究不是“没数据”,而是“数据链路断了”
如果你服务过CAR-T或罕见病项目,你会很快意识到一个现实:研究的难点往往不在“做不做研究”,而在“数据能不能持续地产生、持续地被证明、持续地可追溯”。很多团队一开始把问题理解成“随访难”“患者不配合”“中心太分散”,最后发现真正卡住的是同一个底层矛盾——患者全生命周期的数据链路断了:信息采集不连续、关键节点缺数据;研究过程留痕不完整,复盘无法自证;任务执行无法闭环,脱落率居高不下;数据标准不统一,后期清洗成本飙升;对外输出证据时材料组织耗时且风险高。
把“研究管理”重新理解为三件事
- 患者全生命周期运营:让数据持续产生
- 研究过程留痕:让数据持续可信
- RWS数据底座:让数据持续可用
一、为什么创新药更需要“全生命周期”
在CAR-T、罕见病、肿瘤等场景里,患者从入组、治疗、随访到长期观察,涉及多角色、多触点、多时间跨度。一旦你把患者当作“研究对象”,而不是“被持续服务的人”,随访就会迅速失控。全生命周期管理的核心,不是“做更多随访”,而是让每一次触点都能沉淀数据:入组前的基础信息与知情同意留痕;用药/治疗节点的关键指标采集;不良反应/并发症处理的记录闭环;依从性管理与提醒机制;患者反馈与生活质量记录;退出、失访的原因归因与补救。
二、研究管理最常见的3个断链点
- 采集不稳定 → 脱落率高:把随访变成机制(ePRO、自动提醒、任务闭环)
- 数据标准不统一 → 清洗成本高:采集端标准化(字段模板、必填规则、校验规则、版本控制)
- 过程留痕不足 → 证据输出风险:采集、审核、变更、追溯全流程留痕(可追溯、可解释)
补充:IIT量表与问卷支持(稳妥版表述)
在IIT(研究者发起临床研究)与上市后研究场景中,我们不仅支持患者全生命周期随访管理,也支持围绕不同适应症配置对应的量表与问卷体系。平台可按研究方案配置患者自评(如症状、生活质量、依从性等)、随访事件记录与研究专用问卷,并结合ePRO采集、定时触发、自动提醒、缺失追补、版本管理与全流程留痕,确保量表数据“采得到、不断链、可追溯、可质控”,更稳地支撑研究分析与证据输出。
三、RWS数据底座应该长什么样
- 数据采集:ePRO/随访、中心数据对接、文件管理
- 数据治理:字段标准、质量校验、缺失管理、版本管理
- 合规与追溯:权限、审计轨迹、操作日志(可解释)
- 分析与报告:阶段性分析与输出模板
- 患者运营联动:服务记录回流研究数据链

四、落地路径:先闭环,再规模化
- 第1步:选一个高价值项目跑通闭环(随访周期长、脱落率高的项目优先)
- 第2步:固化模板与指标(字段模板、SOP、质量规则、异常处理)
- 第3步:扩到多项目、多中心(规模化不崩)
结语
从CAR-T到罕见病,研究管理最终都会回到患者全生命周期。只有把患者运营、过程留痕和RWS底座做成闭环,你才有能力持续地产生可用证据,支撑适应症拓展与商业化决策。
行动号召
回复“RWS清单”,领取《RWS数据底座建设清单(从采集到追溯)》与项目落地三步法模板。