
要点先看:CDE 发布《抗肿瘤药物生物等效性及药代动力学(BE/PK)比对研究受试者人群选择考虑》(2026年第22号)后,肿瘤药 BE/PK 比对研究‘选健康人还是选患者’不再是经验判断,而需要以风险-获益评估与科学可表征为依据,形成可追溯、可复核、可导出的合规材料。

一、这份通告解决的核心问题是什么?
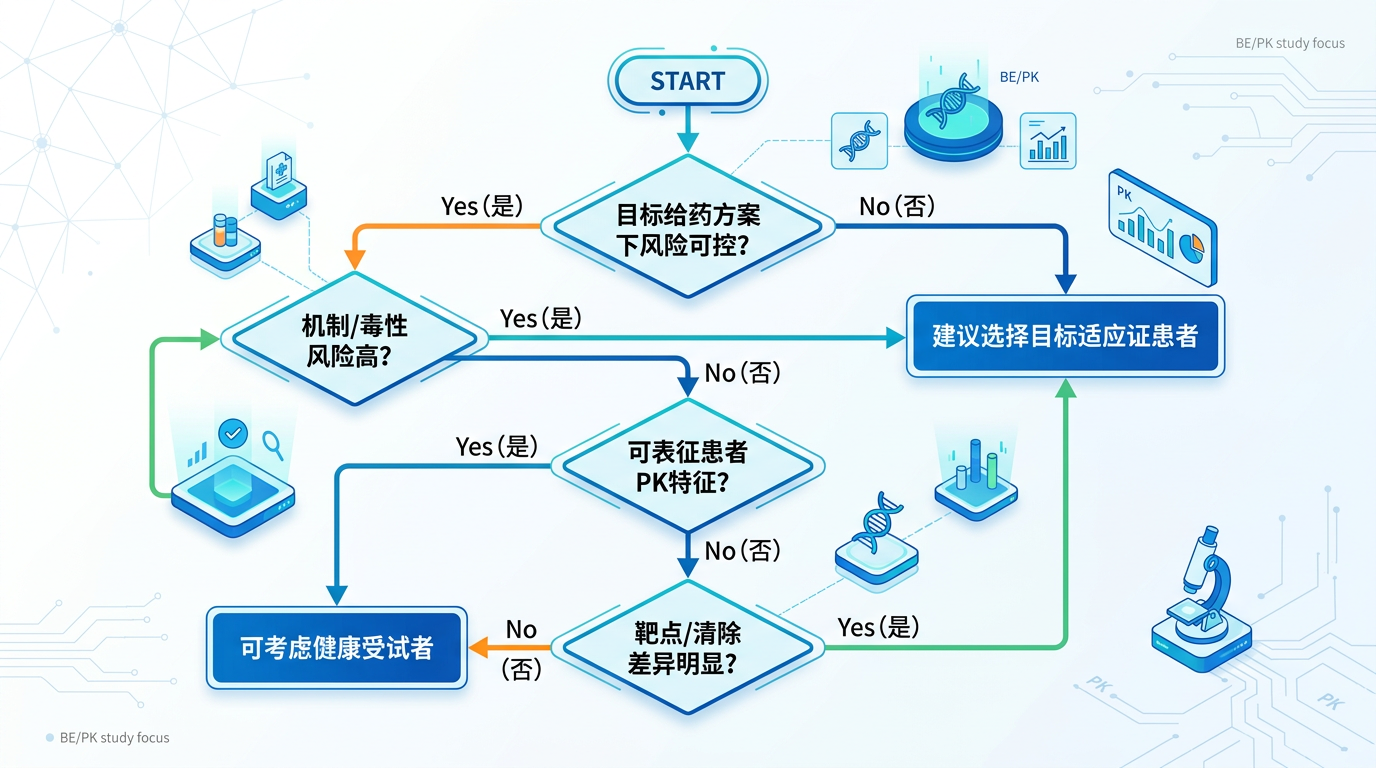
不同类型抗肿瘤药物安全性风险差异很大。CDE 给出了受试者人群选择的原则与考虑框架:在目标临床给药方案(剂量、频率)下,若健康受试者风险可控且能充分表征目标适应证患者 PK 特征,可考虑健康受试者;否则应选择目标适应证患者。
二、受试者选择的关键判断(可直接落地为内部清单)
- 风险是否可控?(机制/毒性风险、对正常细胞/器官损害、严重不良事件可逆性等)
- 是否可表征患者PK特征?(靶点表达、清除机制、耐受性、肿瘤负荷影响等)
- 健康人数据是否足以证明BE/PK相似性?
- 患者研究是否存在潜在获益?(风险-获益角度)
三、申办方最小材料包:把‘选人’做成证据链
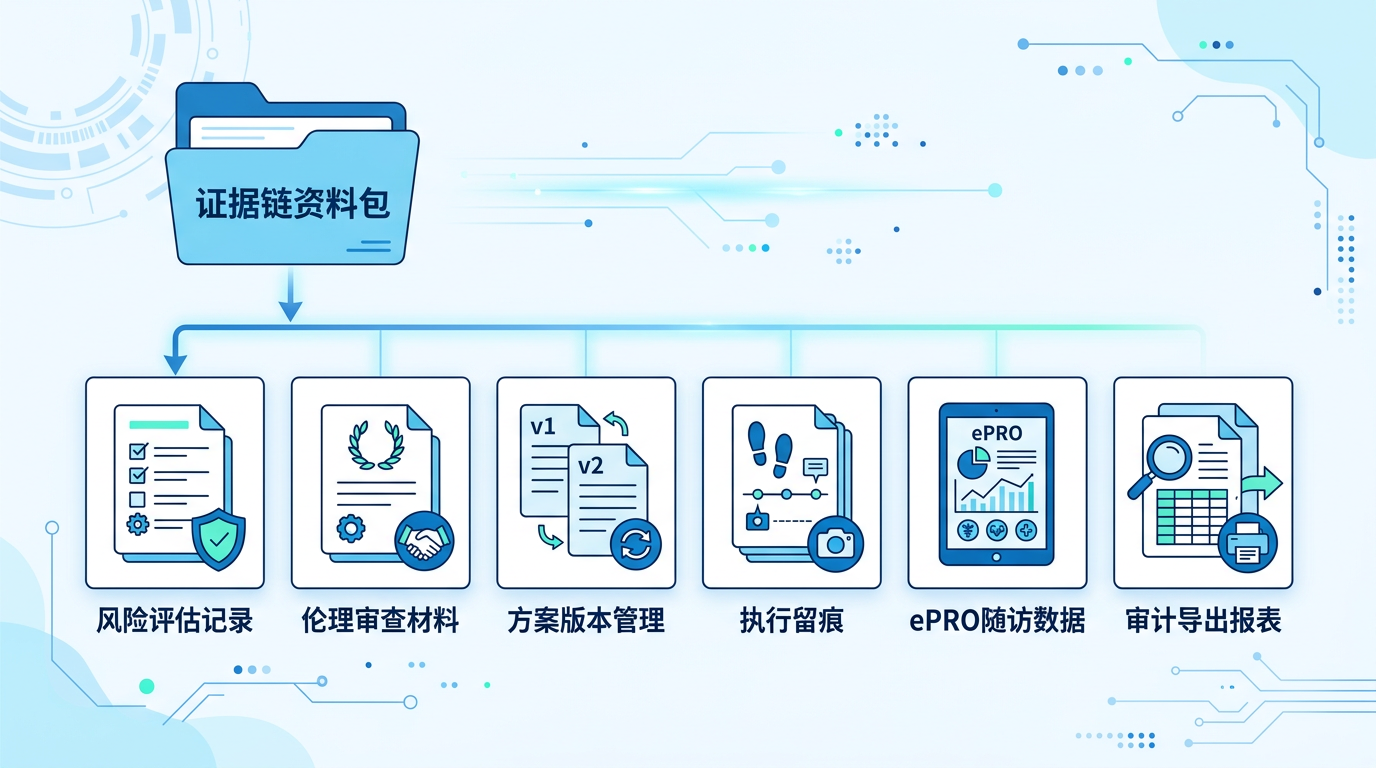
建议把受试者选择从‘口头解释’升级为‘可审计材料包’,至少包括:
- 风险评估记录:依据非临床/临床/上市后信息(如有)形成可追溯结论
- 伦理审查材料:受试者保护、风险控制措施、持续审查安排等
- 方案版本管理:制度/规则/执行版本可回溯
- 执行留痕:关键节点留痕(审批、授权、变更、异常处置)
- 数据采集与完整性:ePRO/随访降低脱落,提高数据可用性
- 审计导出:按事项/时间/责任人维度分钟级导出证据包
四、FAQ
Q1:健康受试者一定不能做吗?
A:不是。关键是目标给药方案下风险可控,且数据能充分表征患者PK特征,并形成可追溯的评估记录。
Q2:为什么这会影响稽查/审计?
A:受试者选择属于关键科学与伦理决策点,检查时常被追问‘为什么选这类人群’,需要能拿出可复核的材料与留痕。
五、CTA(行动号召)
- 预约30分钟 Demo:演示‘节点留痕 → 数据采集 → 证据链导出’闭环
- 领取资料包:《BE/PK受试者选择合规要点清单》《伦理与风险评估记录模板》《审计导出字段字典(示例)》
六、作者介绍 / 关于药智云
药智云聚焦生命科学企业的数据合规与可审计证据链建设,覆盖临床研究数据采集(ePRO/随访)、过程留痕与分钟级证据包导出。
191-5772-9499|https://www.yaozhi.cloud