
一句话结论
药企数智化建设下一阶段真正要升级的,不只是系统数量、流程电子化程度和报表丰富度,而是业务过程是否真正可验证。因为在“AI+药品监管”持续推进的背景下,未来监管越来越不会只满足于“有记录”,而会越来越关注:记录是否真实、过程是否连续、结果是否能被交叉验证、异常是否能被及时识别。
为什么系统越来越多,心里却并不更踏实?
这几年,很多药企都在持续推进数智化建设:审批流程上了线,会议管理有了系统,报销和费用有了电子化流转,资料开始上传归档,业务越来越多地沉淀到线上。按理说,系统越来越多,企业应该更轻松、更有底气才对。但现实恰恰相反,一到检查、审计、飞行检查、专项核查,团队还是容易紧张。核心原因是:很多企业做到了“留痕”,但还没有真正做到“可验证”。
什么叫留痕?什么又叫可验证?
留痕,解决的是“有没有记录”,例如有审批流、有表单、有签到、有照片、有会议资料、有报销单据、有系统操作日志。但留痕本身只能说明有记录存在,不天然等于记录之间能串起来、内容一定可信、过程一定能被还原。可验证则更进一步,它要求整个业务过程中的关键节点之间能够互相衔接、互相印证、形成闭环,能够清楚回答谁发起、谁审批、谁执行、何时何地发生、形成了哪些资料、费用和结果是否对应,以及是否存在断点、补录、异常或逻辑冲突。
为什么AI+药品监管会放大这个问题?
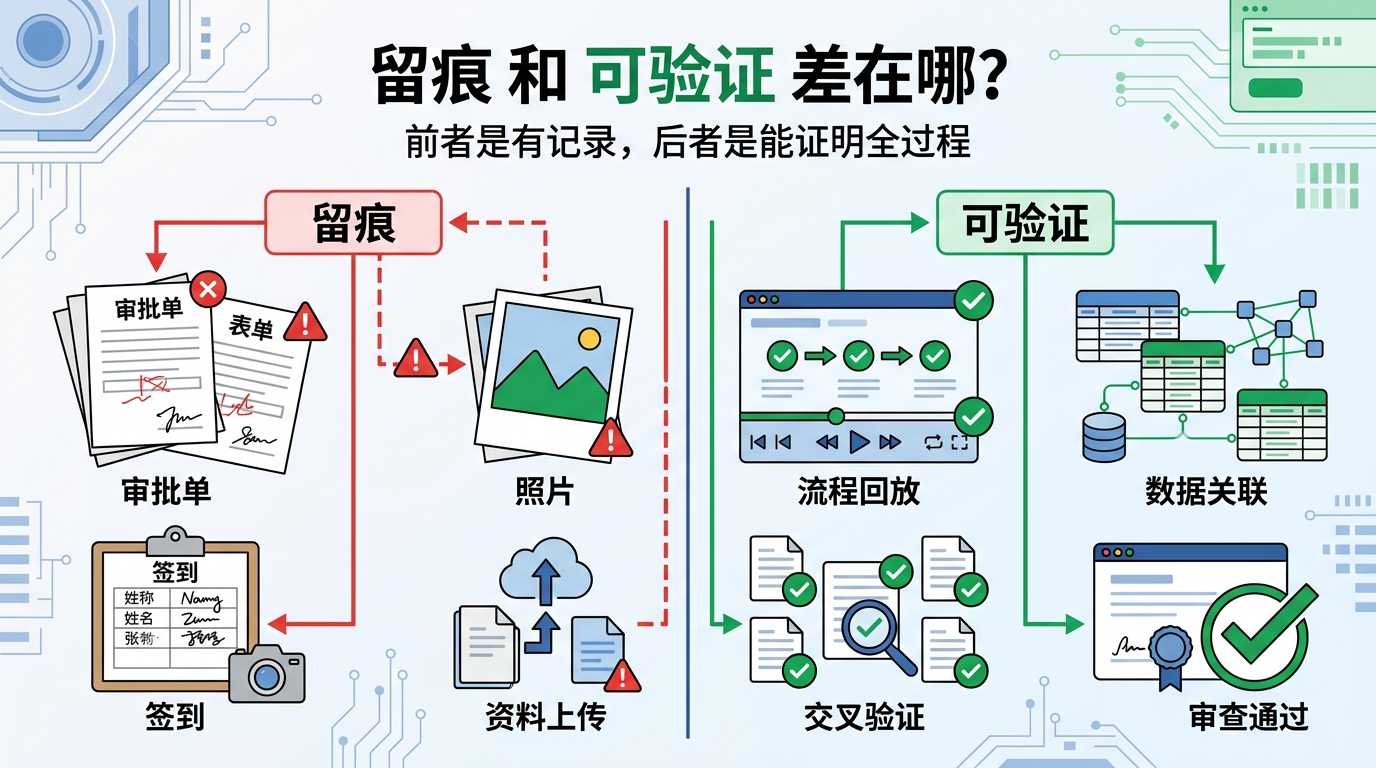
未来监管关注点会越来越从“有没有材料”转向“材料之间能否形成逻辑一致的全过程证明”。资料很多但互相之间无法印证、表面完整但链条存在断点、记录存在但形成时间和执行时间不一致、多个系统之间口径不同、线下动作与线上记录无法对应,这些问题过去还能靠人工解释和补材料缓冲,但在更强调数据关联和过程还原的监管环境下,缓冲空间会越来越小。
为什么看起来有记录,并不等于真的可审查?
很多企业表面上已有很多记录:会议有签到、学术活动有审批、终端执行有照片、流向数据有台账、患者服务有回访记录。但真正到审查时,问题常常出在“链条断裂”上。审批和执行之间对不上,执行记录和费用记录之间没有形成闭环,会议资料、讲者信息、现场留痕无法快速互相验证,流向数据和返利计算规则之间缺少清晰追溯路径,终端行为上传了图片但真实性、时间性、连续性难验证。企业不是没有记录,而是记录无法快速支撑“审查级”验证。
药企下一阶段最该优先补哪4项能力?

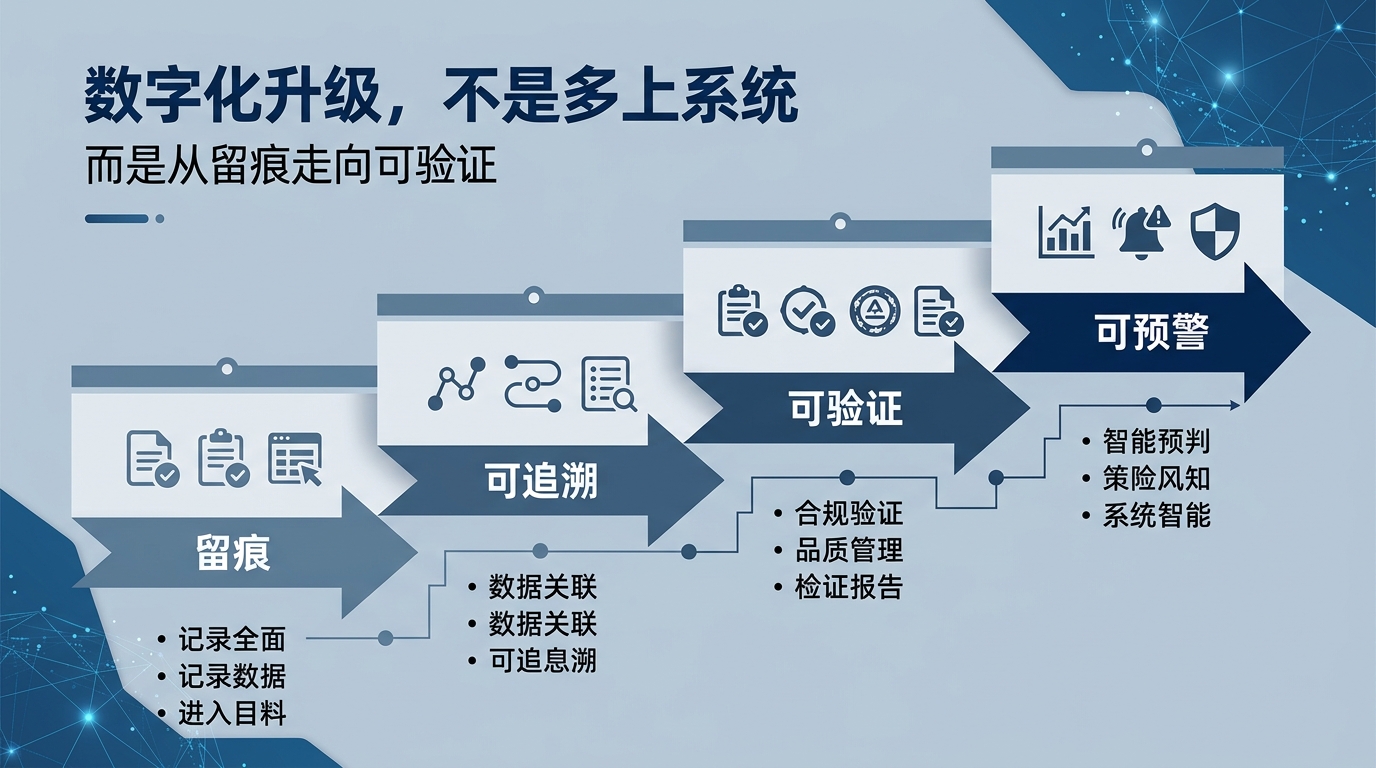
- 结构化数据能力:让扫描件、图片、Word、Excel、纸质单据等碎片化数据变成可查、可比、可串、可预警的数据资产。
- 流程可追溯能力:让谁发起、谁审批、谁执行、何时发生、在哪里发生、形成什么结果形成清晰的前后关系。
- 完整证据链能力:让审批、执行、签到、资料、费用、结果彼此支撑,形成真正可验证的闭环。
- 风险前置识别能力:不要等检查来了再发现问题,而是在日常管理中识别断点、识别异常、识别高风险动作。
哪些业务场景最能体现差距?
最典型的包括学术会议与讲者服务、渠道流向与返利结算、终端执行与药店管理、患者服务与RWS数据采集。这些场景共同特点是节点长、参与者多、资料复杂、后续经常需要回溯。如果只是“留了资料”,但没有把立项、审批、执行、费用、归档、审查串起来,那么系统价值就仍然有限。
药智云真正能提供什么?
药智云真正能提供的,不只是“留痕工具”,而是帮助企业从留痕走向验证能力升级的数智化底座:在学术推广与合规管理场景中,把会议、讲者、执行、费用、审查等环节串成更完整的证据链;在流向与返利结算场景中,把数据整合、OCR识别、异名匹配、返利追溯这些能力做成清晰闭环;在终端与患者/RWS场景中,也能把现场动作与服务过程沉淀成更可信、更可回溯的数据记录。
结语
如果说过去药企数智化建设的重点,是把流程搬上线、把资料沉淀下来,那么接下来更重要的一步,就是让这些流程和资料真正具备验证价值。未来企业之间拉开的差距,不会只体现在系统上得多不多、表单做得细不细,而会更体现在数据是不是结构化的、过程是不是连续可追溯的、证据是不是闭环的、风险是不是能提前识别的。