
对于管理要求更高、跨部门协同更复杂的药企来说,合规压力往往并不来自某一个单独环节,而是来自多个环节叠加后的管理复杂度。培训要有记录,活动要有留痕,材料要有审核,版本要能追溯,制度更新后还要能证明已经覆盖到对应人群。平时看上去都在运转,但一到飞检、审计或专项复核场景,企业最怕的常常不是没做,而是证据链不完整。
因此,高标准药企真正需要的,不只是把资料收得更全,而是把关键动作的证据链前移,让高风险、强监管、跨部门的核心流程在发生时就被标准化记录。只有这样,合规管理才能从事后找材料,走向过程可证明。
为什么高标准药企更容易陷入做了很多、证据却不完整
越是管理严格、活动频繁、跨部门协同复杂的高标准药企,越容易遇到另一类问题:不是没做,而是做了很多之后,很难在短时间内把全部证据完整、准确、一致地拉齐。
培训归培训系统,活动归活动团队,医学审核归医学事务,市场传播有自己的材料流转,合规和内审又有独立的复核要求。一旦进入飞检、审计或专项复核场景,企业被要求交付的不是零散记录,而是一条逻辑完整、责任清晰、时间可追溯的证据链。
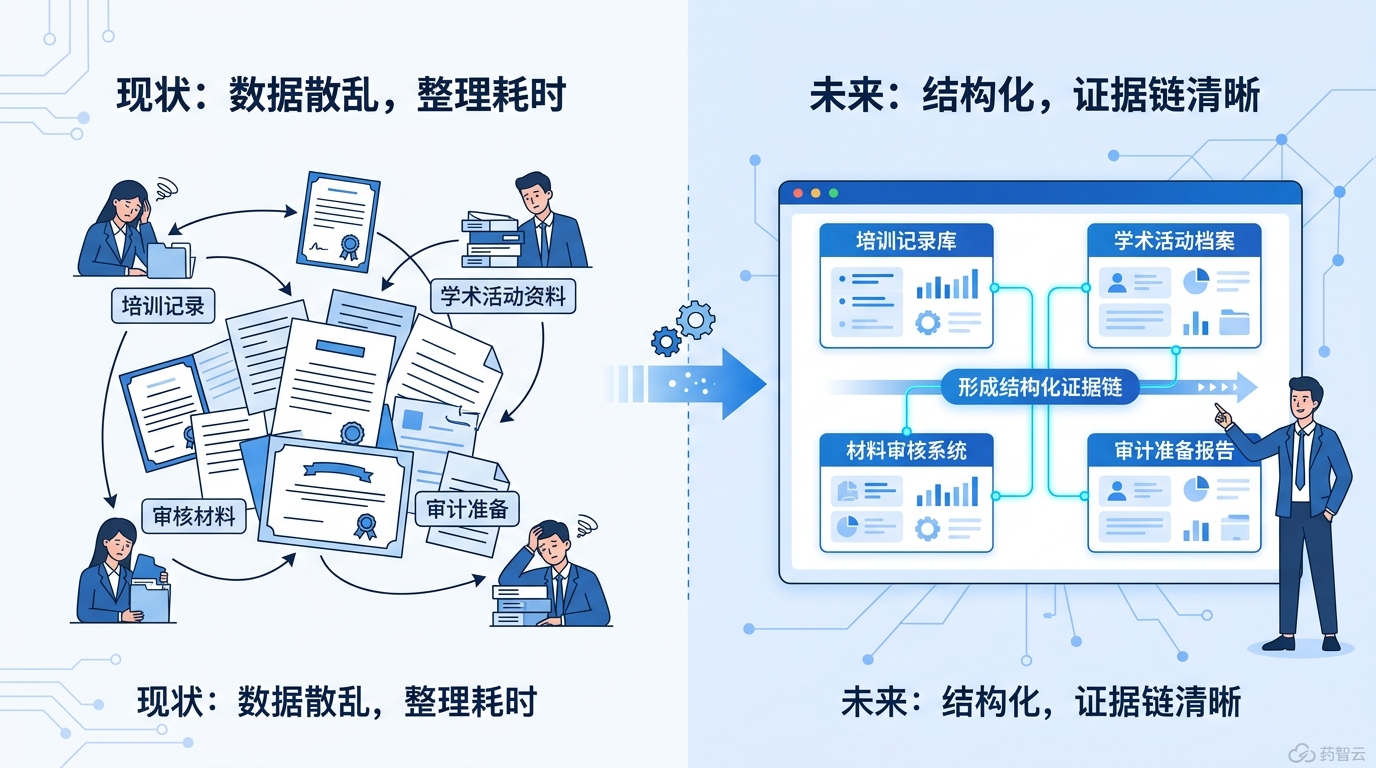
学术推广与合规管理最常见的四个断点
第一类断点,是活动记录在,支撑材料不全。第二类断点,是医学审核做了,但版本与流程留痕不完整。第三类断点,是培训开展了,但认证与执行证据分散。第四类断点,是审查需要跨部门拼接,准备周期长。
这些问题的共同点,不在于企业没有流程,而在于关键动作没有在发生时被统一留痕、统一追溯、统一归集。
为什么证据链必须前移
很多企业在面对检查压力时,第一反应是把归档做得更细一点。但现实是,合规管理的核心从来不是事后归档,而是过程留痕。
所谓证据链前移,意思不是增加更多表单,而是让高风险动作在发生时就被标准化记录,让关键审批、培训、活动、材料审核在当下完成留痕,而不是等到事后靠人工回忆和补材料。这种前置化管理方式,真正解决的是组织在高压审查场景中的脆弱性。
药智云可以怎样承接这类场景
在这类场景下,药智云更适合承接的,不是单纯多做一个归档工具,而是帮助企业从资料归集式合规,转向前置化证据链管理。
通过合规审查系统,可以承接活动留痕、材料审核、审查准备、证据链归集等关键环节,把原本分散的动作尽量纳入统一逻辑下管理。这样做的价值,是优先把那些高风险、强审查、跨部门的关键动作先标准化、先留痕、先打通。
结语
对于高标准药企来说,真正决定合规治理成熟度的,往往不是制度写得多完整,而是关键动作能否在真实业务场景中被持续、准确、可追溯地证明。把证据链前移,不只是为了应对一次飞检或审计,更是为了把合规能力从被动应对升级为前置治理。
如果您的团队也在面对学术活动、材料审核、培训留痕和审查准备压力,欢迎与药智云团队交流。